El camino que recorren los pacientes con enfermedad inflamatoria intestinal (EII) y sus familiares después de ser diagnosticados con colitis ulcerosa o enfermedad de Crohn es arduo. Asumir la noticia que han recibido, acudir a todas las consultas de especialistas, realizarse las pruebas pertinentes para conocer el alcance de la enfermedad o el tiempo que se tarda en ajustar y establecer el tratamiento correcto, son solo algunos de los obstáculos y retos que deben superar. Y, precisamente, acertar y recibir el tratamiento adecuado es uno de los puntos más complejos al que se tiene que enfrentar el paciente.
Noticias
Granulocitoaféresis en pacientes con colitis ulcerosa
10 de enero, 2023
Adacolumn

Centrándonos en el caso de la colitis ulcerosa, patología que produce la inflamación del recto y el colon, el paciente sufre recidivas con brotes de actividad más o menos intensos, y más o menos duraderos. Los fármacos que actualmente forman parte del arsenal terapéutico del profesional sanitario para tratar a los pacientes, buscan inducir la remisión de esos brotes y mantener inactiva la EII para mejorar la calidad de vida del enfermo. Y, por supuesto, siempre con la mayor eficacia y seguridad posible.
Teniendo en cuenta que algunos pacientes no responden a los tratamientos convencionales o incluso que debido a su perfil no pueden hacer uso de ellos, los profesionales sanitarios han visto en la granulocitoaféresis (GMA) un aliado terapéutico con garantías de éxito en pacientes con colitis ulcerosa. Y esto se debe a que la técnica reduce la cantidad de células inflamatorias existente en el torrente sanguíneo sin necesidad de introducir un fármaco en el paciente.
¿En qué consiste la granulocitoaféresis?
Como hemos escrito en líneas anteriores, la GMA es un tratamiento no farmacológico cuyo fundamento es pasar la sangre del paciente a través de un dispositivo extracorpóreo con la finalidad de eliminar de ella aquellos componentes patógenos que condicionan o perpetúan la enfermedad y de esto modo contribuir a su tratamiento.
Uno de los sistemas de granulocitoaféresis comercializados en Europa es un sistema que se compone de una columna o filtro con esferas de acetato de celulosa que permite la adsorción selectiva de un 65% de granulocitos, un 55% de monocitos/macrófagos y un 2% de linfocitos, eliminándolos así del torrente sanguíneo. El procedimiento consiste en extraer la sangre de la vena cubital del paciente, que circula por el circuito y la columna de adsorción para ser depurada, y se reinfunde a través de la vena cubital contralateral (fig.1, incluimos imagen del proceso).
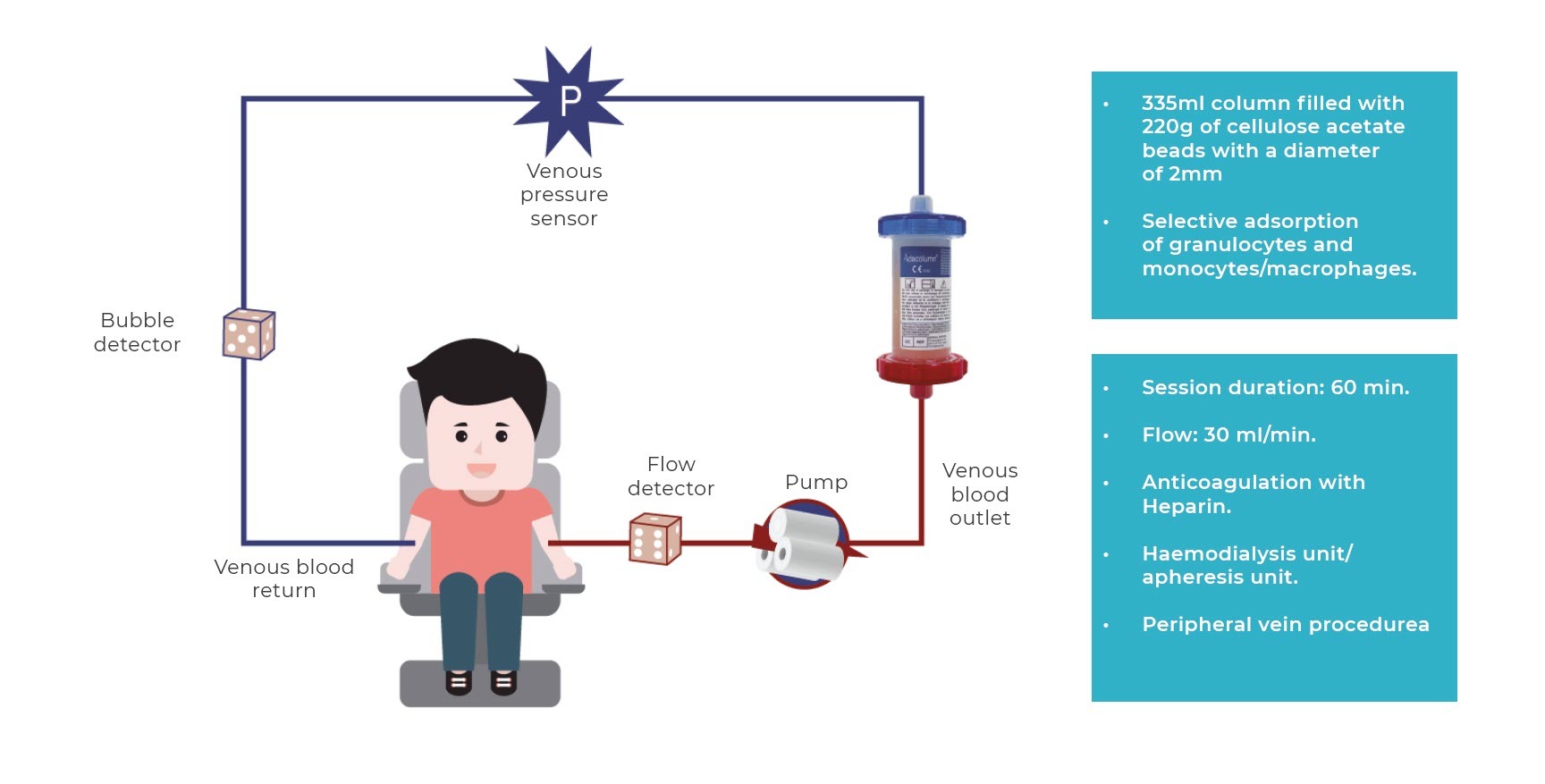
El procedimiento se realiza en unidades de hemodiálisis o bancos de sangre, aunque tras una formación adecuada se puede realizar en unidades de tratamiento en régimen de hospital de día. La pauta de aplicación de la técnica (frecuencia y número de sesiones), va desde 5 sesiones a 10 (1 o 2 por semana) de 60º más minutos de duración, aunque la práctica clínica real en la mayoría de hospitales consiste en una inducción de 10 sesiones (las primeras 3 semanas 2 sesiones/semana para acelerar la respuesta y luego 1 sesión semanal hasta completar las 10) y de mayor duración (normalmente de 90 minutos), ya que se ha observado que este régimen es seguro y bien tolerado, obteniéndose mejores resultados clínicos.
Sin embargo, la única limitación práctica para su realización es la mala accesibilidad para canalizar vías periféricas, lo que podría obligar a colocar una vía central.
En la actualidad aún no se conoce de forma exacta el mecanismo de acción de la GMA. Se sabe, no obstante, que los granulocitos y los monocitos/macrófagos se encuentran elevados y activados en sangre periférica en muchas de las enfermedades autoinmunes, que su número se correlaciona con la actividad y con la gravedad de la enfermedad y que desempeñan un papel clave en la inmunopatogénesis en tanto que producen elevadas cantidades de citocinas proinflamatorias responsables de la lesión tisular.
Se cree que el mecanismo principal de adsorción de la GMA está relacionado con la activación de la cascada del sistema del complemento y con la inducción de la adhesión de los granulocitos a la columna.
Los leucocitos que expresan el receptor Fc gamma (FcγR) y receptores del complemento (Mac-1, CD11b/CD18) se adhieren a las cuentas de acetato de celulosa a través de la activación del complemento. De este modo, la disminución del reservorio de granulocitos activados en la circulación sistémica se compensa con la movilización, desde la médula ósea al torrente circulatorio, de granulocitos jóvenes, no activados (CD10–), sin capacidad de migrar al foco inflamatorio.
Asimismo, se produce un cambio funcional en los monocitos activados, que expresan marcadores CD14+CD16+, lo que en su conjunto conlleva una reducción de la producción de citocinas proinflamatorias y un incremento de mediadores antiinflamatorios circulantes; en definitiva, un fenómeno de inmunomodulación y consiguientemente una reducción del infiltrado inflamatorio y del daño tisular.
La consecuencia directa de la eliminación de leucocitos del sistema circulatorio es la movilización por parte de la médula ósea de leucocitos jóvenes inactivados que no pueden migrar al foco inflamatorio. Adicionalmente el paso de la sangre a través de la columna, además de disminuir el número total de células inflamatorias en la sangre también produce cambios en la superficie de las que retornan al organismo induciendo una serie de cambios a nivel inmunológico que promueven la activación de mecanismos antinflamatorios que estaban inhibidos, poniendo en marcha la resolución de la inflamación. Con ello, además de producir inmunomodulación (cambio que se produce en el sistema inmunitario), se reduce la inflamación y el daño tisular (de las células) en la mucosa intestinal.
¿En qué pacientes está indicado el uso de la GMA?
Actualmente, existe un arsenal terapéutico muy amplio para el tratamiento de la EII aunque en una proporción de pacientes estas medicaciones son ineficaces o presentan efectos adversos2. Por lo tanto, se necesitan otras opciones terapéuticas para controlar la progresión de la enfermedad y evitar intervenciones quirúrgicas.
Otra alternativa para el tratamiento de esta patología en determinados escenarios es la GMA. Esta técnica puede aplicarse en diferentes situaciones, incluyendo aquellos pacientes que no responden adecuadamente a los tratamientos farmacológicos convencionales, o presentan un curso corticodependiente, prevención de recidiva y en los que se plantea iniciar tratamiento inmunosupresor o biológico3,4.
A pesar de buscar el mejor tratamiento para cada caso, existe un alto porcentaje de pacientes con colitis ulcerosa que no responden a los tratamientos convencionales, ya sea a aquellos basados en corticoides o en inmunomoduladores (IMM) tiopurínicos (Ardizzone et al, 2006) o a la terapia anti-TNF. Hasta hace unos años, cuando un profesional sanitario se encontraba en esta situación en la que los medicamentos no lograban mejorar la situación de los pacientes, la opción más utilizada para tratarlo y mejorar su calidad de vida era la cirugía.
Pero en las últimas décadas han surgido otras alternativas de tratamiento en pacientes con colitis ulcerosa, como la GMA, que son más seguras y que pueden aplicarse a los siguientes pacientes1:
- Pacientes adultos con colitis ulcerosa corticodependientes tras el fracaso, intolerancia o riesgo elevado de los tratamientos inmunomoduladores y/o biológicos2.
- Pacientes de edad avanzada con comorbilidades.
- Pacientes embarazadas.
- Pacientes pediátricos con colitis ulcerosa.
Las contraindicaciones son:
- Cifra de granulocitos inferior a 2000/Ml
Las advertencias son:
- Alergia a la heparina y trombopenia dependiente de heparina
- Anemia significativa (Hb < 8 g/dL)
- Coagulopatía grave
- Infección activa
- Enfermedad cardiaca o renal grave
Precauciones:
Precaución en situaciones de hipercoagulabilidad (fibrinógeno > 700 mg/mL) o deshidratación (diarrea o procesos febriles recientes). Deben corregirse previamente estos factores.
GMA, significado de eficacia y seguridad en el tratamiento de la CU
Si hay dos características que definen la GMA son su seguridad y su eficacia. Según recoge el Proyecto Prodiggest3 esta opción terapéutica ha sido objeto de estudios y metaanálisis que permiten describirla como una alternativa eficaz y segura para los pacientes.
Por un lado, se describe la GMA como muy segura para los pacientes con colitis ulcerosa porque los efectos adversos de los tratamientos convencionales desaparecen. En este caso los efectos secundarios son en su mayoría leves y transitorios, por lo que el paciente puede continuar con el tratamiento. Entre ellos destacan la cefalea, los escalofríos, la febrícula, los mareos, la fatiga, las mialgias, las palpitaciones, la hipotensión o el enrojecimiento. En muchos casos los efectos adversos están más relacionados con la técnica de aféresis que con el propio tratamiento de GMA (problemas con las vías…etc), de ahí la importancia de que sea realizada por profesionales expertos.
Por otro lado, además de su eficacia en pacientes pediátricos, embarazadas, ancianos o pacientes corticodependientes y corticorrefractarios, existen otros escenarios donde la GMA es eficaz. Por ejemplo, se ha comprobado que puede ser un tratamiento de primera línea con una tasa de inducción a la remisión del 70% en colitis ulcerosa distal con actividad leve moderada (Yamamoto et al 2004) y hasta el 80% en pacientes con enfermedad poco evolucionada, naïve a esteroides (Takemoto et al 2007), tal y como se recoge en el Proyecto Prodiggest.
Además, es una opción que puede prevenir la recidiva en determinados casos de pacientes con un alto riesgo de sufrir brotes de forma recurrente y difíciles de controlar. En este sentido, se puede establecer una duración media de la remisión clínica en pacientes con colitis ulcerosa obtenida con la GMA de 10 meses (Ljung et al 2007) pudiendo llegar a ser incluso muy superior al año cuanto más inicial sea la enfermedad o menos tratamientos se hayan administrado al paciente con anterioridad (corticoides, tiopurinas, biológicos…etc) a la GMA.
- https://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinalhttps://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinal
- Tratamiento de la colitis ulcerosa en pacientes dependientes de corticoides y fracaso previo a biológicos: Adacolumn® – Adacyte
- https://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinal
- Dignass A, Lindsay JO, Sturm A, Windsor A, Colombel JF, AllezM, et al. Second European evidence-based consensus on thediagnosis and management of ulcerative colitis part 2: Currentmanagement. J Crohns Colitis. 2012;6:991—1030.
- Dignass A, Akbar A, Hart A, et al. Safety and efficacy of granulocyte/monocyte apheresis in steroid-dependent active ulcerative colitis with insufficient response or intolerance to immunosuppressants and/or biologics [the ART trial]: 12-week interim results. J Crohns Colitis. 2016;10:812–820.
- Dittrich K, Richter M, Rascher W, et al. Leukocytapheresis in a girl with severe ulcerative colitis refractory to corticosteroids, infliximab, and cyclosporine A. Inflamm Bowel Dis. 2008;14:1466–1467.
ContáctanosPara solicitar información adicional
Contáctanos

